L'imagerie médicale est aussi un élément essentiel à la recherche clinique, l’étude des maladies et la mise au point de nouveaux traitements. Il existe de nombreuses techniques d’imagerie complémentaires. L'imagerie recouvre à une grande variété de technologies développées grâce à l'exploitation des grandes découvertes de la physique du 20e siècle :
- Les ondes radio et rayons X
- La radioactivité de certains éléments
- Les champs magnétiques.
Représentation de 38 faisceaux longs de la substance blanche cérébrale (chaque couleur code 1 faisceau). © CEA/Neurospin
L’objectif est non seulement de diagnostiquer les maladies, suivre leur évolution, découvrir leur fonctionnement, mais aussi de mieux les soigner. Des techniques sont mises au point pour localiser les foyers d’infection, les cibler et activer les principes actifs de médicaments uniquement à l’endroit souhaité. Ou encore, de détruire les cellules bien localisées grâce à des ondes de cisaillement émises par un échographe, et donc sans acte chirurgical. Le développement de l’IRM pour la recherche sur le cerveau ouvre également les perspectives d’une compréhension de plus en plus fine de cet organe très complexe.
Un peu d'histoire
L’imagerie médicale a fait son apparition avec la
découverte des rayons X par Wilhelm Röntgen (physicien allemand) en 1896. Très vite, l’intérêt d’une telle découverte pour la médecine se développe et Antoine Béclère, chef de service à l’hôpital Tenon à Paris, acquiert en 1897 un radioscope. Les premiers dépistages de la tuberculose y sont effectués grâce aux radiographies des poumons. L’imagerie médicale se développe au cours de la Première Guerre mondiale, avec notamment la mise en place, par Marie Curie, de voitures radiologiques qui sillonnent les champs de bataille pour repérer les éclats d’obus chez les soldats blessés.
En 1934, la découverte de la radioactivité artificielle par Frédéric et Irène Joliot-Curie ouvre la voie au développement des
radioéléments de brève durée de vie. Ces derniers, associés à des molécules biologiques utilisées comme traceurs, ont permis la découverte du fonctionnement de certains organes. Depuis, l’imagerie médicale n’a cessé d’évoluer, de se perfectionner et de proposer des technologies de plus en plus précises, performantes et novatrices.
Les différentes technologies D’imagerie médicale
Radiographie |
Scanner |
Scintigraphie monophotonique |
Tomographie par émission de positons |
Échographie |
Électro-encéphalographie |
Magnétoencéphalographie |
Imagerie par résonance magnétique |
IRM de diffusion |
IRM fonctionnelle
ancre_radiographie
La radiographie
La radiographie repose sur l’utilisation des rayons X qui ont la propriété de traverser les tissus de manière plus ou moins importante selon leur densité. Ainsi, une source émettrice de rayon X est placée devant le corps à radiographier et un détecteur est placé à l’arrière du corps. Les photons émis vont traverser le corps en étant plus ou moins absorbés par les tissus rencontrés sur leur chemin. Cela permet de différencier les os des muscles sur le cliché final.
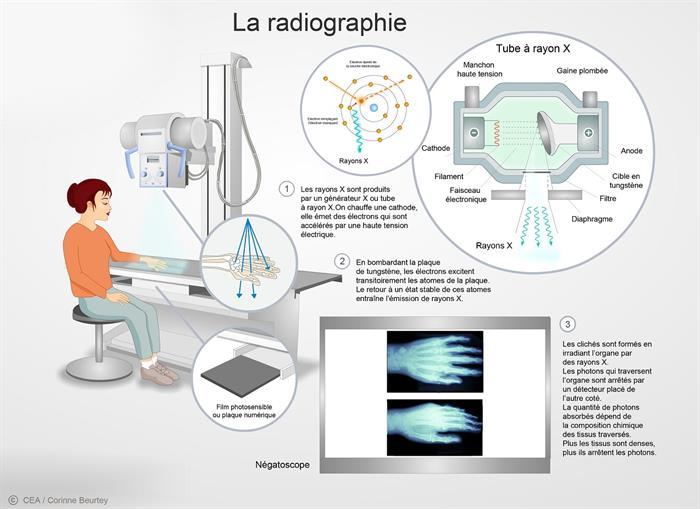
Principe de la radiographie © C. Beurtey/CEA
ancre_scanner
Le scanner
Le scanner repose sur le même principe que la radiologie, c’est-à-dire utilisation d’une source de rayons X et d’un détecteur de part et d’autre du corps étudié.
Il permet d’obtenir des images 3D grâce à une rotation simultanée de la source émettrice de rayons X et du détecteur autour du corps. Les projections intermédiaires en 2D sont traitées par informatique afin d’obtenir des images 3D.
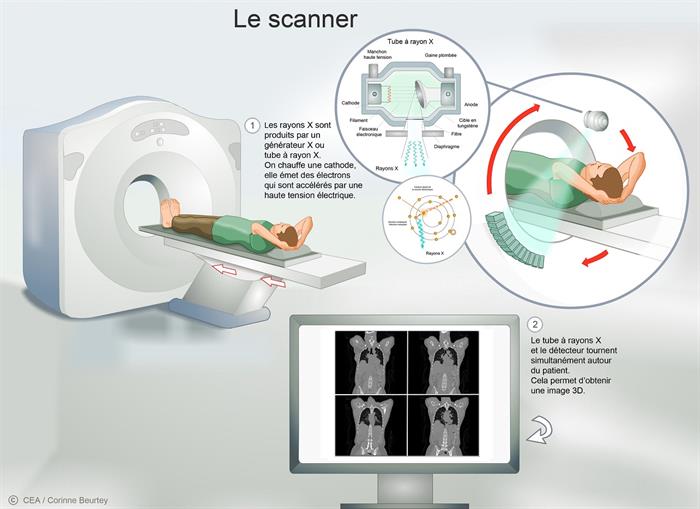
Le scanner © C. Beurtey/CEA
ancre_scintigraphiemonophotonique
La scintigraphie monophotonique
La scintigraphie monophotonique repose sur l’utilisation de deux éléments fondamentaux : un
traceur radioactif
[1] injecté au patient et
une caméra sensible aux rayons gamma. Le traceur, marqué par un atome radioactif qui émet des photons dans toutes les directions, va se fixer spécifiquement sur l’organe à analyser. Les photons émis traversent le corps du patient jusqu’à la gamma caméra. Cette dernière est équipée d’un collimateur
[2] qui ne laisse passer que les rayons parallèles aux espaces aménagés à cet effet.
Leur rôle est de délimiter les points d’émission des photons. La gamma caméra tourne autour du patient afin d’obtenir, après reconstitution informatique, des images 3D de l’organe étudié. Les atomes radioactifs utilisés pour l’imagerie scintigraphie ont une demi-vie courte (6h pour le Tc l’isotope le plus utilisé) et la
radioactivité a disparu au bout de 10 demi-vies.
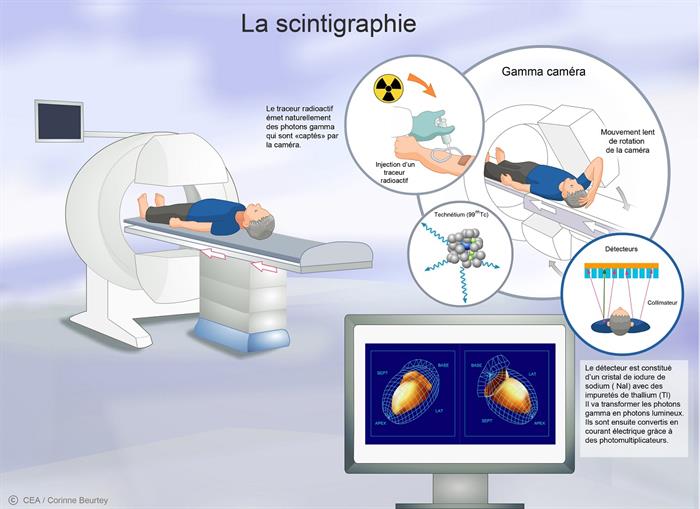
La scintigraphie monophotonique © C. Beurtey/CEA
ancre_tomographieparemissiondepositons
La tomographie par émission de positons (TEP)
La tomographie par émission de positons (TEP) est basée sur l’utilisation d’un traceur marqué par un atome radioactif, le Fluor 18 ou le Carbone 11, qui émet des positons.
Après son injection dans l’organisme par voie intraveineuse, le traceur s’associe à sa cible biologique. Les positons, émis lors de cette association, s’annihilent avec les électrons environnant en émettant deux photons dans des directions diamétralement opposées. Une couronne de détecteurs placée autour du patient va permettre de capter les photons de part et d’autre de la région cible. Le traitement de l’ensemble de ces captures conduira à la reconstitution, au besoin, d’une image 3D de la zone étudiée.
Les atomes radioactifs utilisés pour la TEP ont une demi-vie courte (20 min à 2 h environ selon les isotopes) et l’essentiel de la radioactivité disparaît au bout de 10 demi-vies.
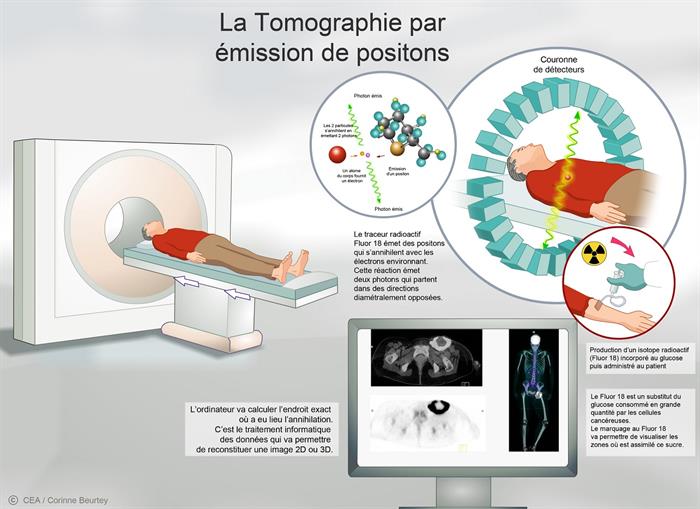
La tomographie par émission de positons (TEP) © C. Beurtey/CEA
ancre_echographie
L’échographie ultrasonore
L’échographie ultrasonore est une modalité d’imagerie médicale qui repose sur l’exposition de tissus à des ondes ultrasonores et sur la réception de leur écho. L’échographe se compose d’un écran et d’une sonde émettrice et réceptrice des ondes (appelée transducteur).
Soumises à un courant électrique, les micro-céramiques à la surface de la sonde vibrent et émettent des ondes ultrasonores. Ces ondes traversent les tissus et y font écho différemment selon leur densité : plus un tissu est dense, plus l’écho est important. Les ondes reviennent au niveau de la sonde, font vibrer les céramiques qui induisent un courant électrique traité par informatique. Ainsi, lors d’une échographie réalisée dans le cas d’un suivi de grossesse, il est possible de différencier le squelette du fœtus, de ses organes, du liquide amniotique…
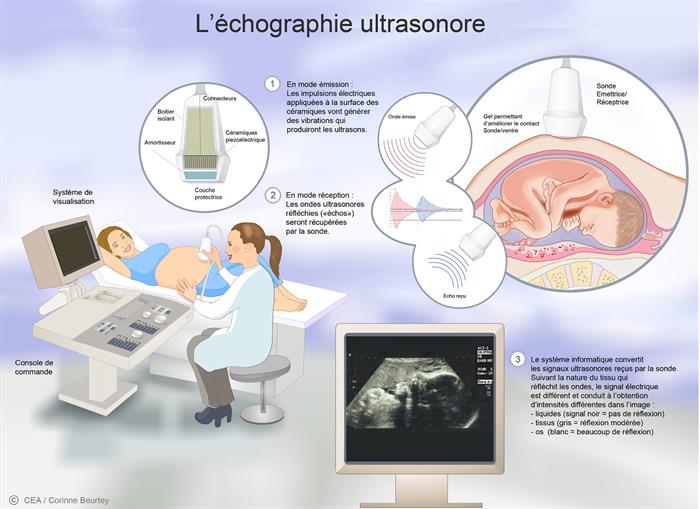
L’échographie ultrasonore © C. Beurtey/CEA
ancre_electro-encephalographie
L’électro-encéphalographie
L’électro-encéphalographie est l'une des technologies d’imagerie les plus anciennes. Elle permet de visualiser, et de localiser, rapidement une activité cérébrale. Pour cela, elle utilise les différences de potentiel [3] qui se créent au niveau des synapses, espaces entre deux neurones où circule l’influx nerveux.
Celui-ci passe d’un neurone à l’autre grâce à la libération de neurotransmetteurs. Ces molécules chimiques vont créer une tension électrique entre les deux neurones qui pourra être mesurée grâce aux électrodes placées sur le cuir chevelu du patient. Le signal détecté résulte des signaux émis par l’ensemble des neurones présents dans la zone du cerveau activée.
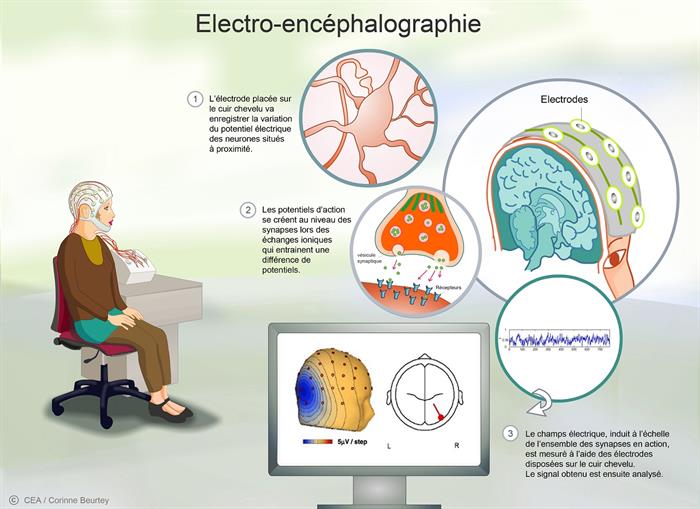
L’électro-encéphalographie © C. Beurtey/CEA
ancre_magnetoencephalographie
La magnétoencéphalographie
La magnétoencéphalographie est une technologie d’imagerie « passive » du cerveau, tout comme l’électroencéphalographie, car elle repose sur la
captation du champ magnétique résultant de l’activité du cerveau.
La circulation de l’influx nerveux le long des neurones équivaut à la circulation d’un signal électrique le long d’un fil conducteur, ici les axones. Un courant électrique induit un champ magnétique perpendiculaire au sens de sa circulation. C’est ce très faible champ magnétique, plus d'un million de fois plus faible que le champ magnétique terrestre, qui va être mesuré grâce à des capteurs appelés SQUID (Superconducting QUantum Interference Device). Appliquant le principe inverse, un champ magnétique induit un courant dans une
bobine, ce courant est ensuite analysé pour visualiser les zones d’activité du cerveau.
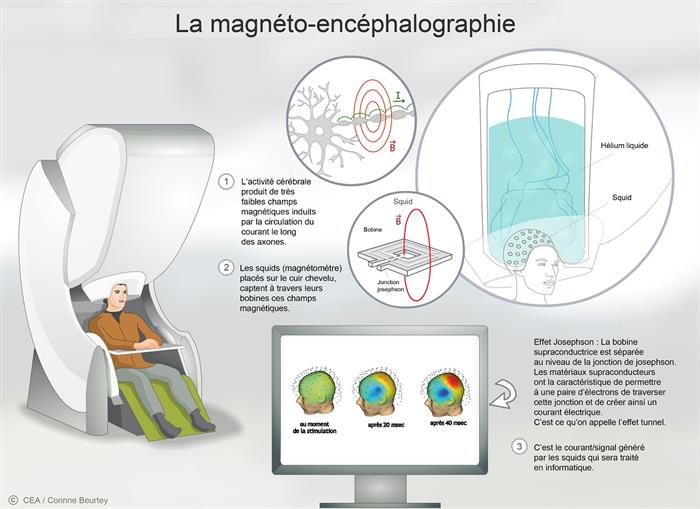
La magnétoencéphalographie © C. Beurtey/CEA
ancre_imagerie-par-resonance-magnetique
L’imagerie par résonance magnétique
L’imagerie par résonance magnétique repose sur les propriétés magnétiques des molécules d’eau qui composent à plus de 80% le corps humain. Les molécules d’eau, plus précisément ses atomes d’hydrogène, possèdent un "moment magnétique", ou
spin, qui agit comme un aimant.
L’appareil IRM consiste à créer un champ magnétique puissant (B0) grâce à une bobine. Le patient est placé au centre de ce champ magnétique, et toutes les molécules d’eau présentes dans le corps vont s’orienter suivant B0. Une antenne placée sur la partie du corps étudiée (ici la tête) va permettre d’émettre et de réceptionner certaines fréquences. A l’émission, la fréquence induite va faire basculer les molécules dans un plan perpendiculaire à B0. Lorsque l’antenne arrête d’émettre, les molécules reviennent à leur position d’origine en émettant à leur tour une fréquence captée par l’antenne. Celle-ci est ensuite traitée comme un signal électrique et analysée par des logiciels. Le signal diffère selon que les tissus observés contiennent plus ou moins d’eau.
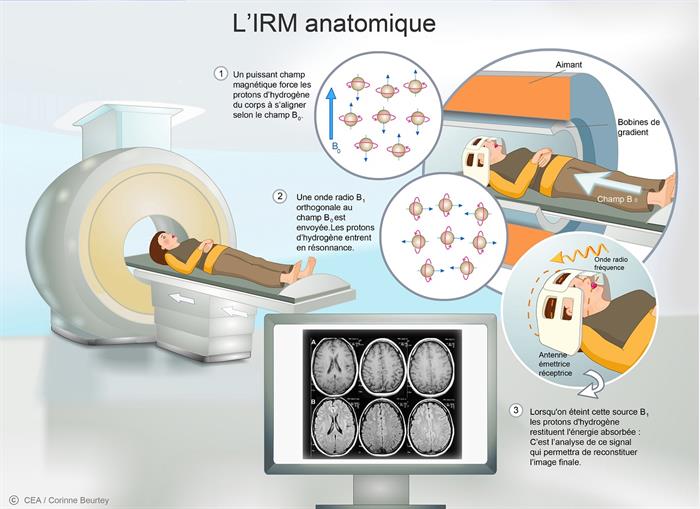
L’imagerie par résonance magnétique © C. Beurtey/CEA
ancre_irm-de-diffusion
L’IRM de diffusion
L’IRM de diffusion repose sur les principes de base de l’IRM tout en
se focalisant sur le déplacement des molécules d’eau présentes à l’intérieur des fibres nerveuses (ou axones).
Ces fibres sont gainées de myéline, principalement constituée de lipide, qui va, en partie, retenir les molécules d’eau à l’intérieur de l’axone. C’est pourquoi, dans un temps donné, les molécules d’eau, qui bougent de manière aléatoire, vont parcourir une plus grande distance lorsque leur déplacement se fera dans le sens de la fibre. L’analyse IRM va ensuite permettre de visualiser le parcours de chacune des molécules et ainsi de reconstituer le réseau de fibres nerveuses à l’intérieur du cerveau.
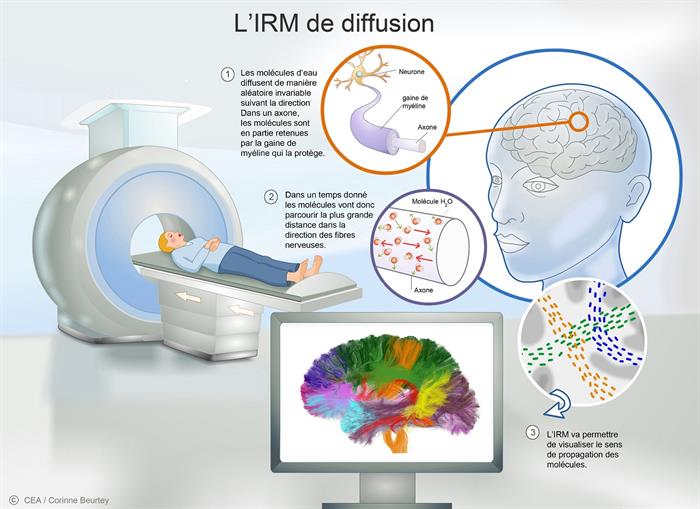
L’IRM de diffusion © C. Beurtey/CEA
ancre_irm_fonctionnelle
L’IRM fonctionnelle
L’IRM fonctionnelle permet de visualiser les zones du cerveau activées par un stimulus présenté ou appliqué au sujet. Par exemple, lorsque l’on demande à la personne de regarder une image, les zones activées dans le cerveau vont recevoir un apport d’oxygène par voie sanguine plus important qu’en l’absence du stimulus.
Les échanges d’oxygène entre le sang et les neurones modifient le signal IRM.
Cette différence de signal IRM entre les états de repos et de stimulation est analysée par informatique. Les images IRM dont le signal est rehaussé correspondent à la zone du cerveau impliquée dans la réponse au stimulus.

L'IRM fonctionnelle © C. Beurtey/CEA
Les progrès attendus de l’imagerie médicale
L'avenir de l'imagerie médicale passera par plusieurs axes d'amélioration, aujourd'hui développés en parallèle :
-
Des instruments plus puissants et possédant donc une meilleure définition. Par exemple, la conception d'aimants créant le champ puissant B0 conduira une définition plus fine des images obtenues par IRM, à la détection d'un signal plus faible.
-
Des agents de contrastes plus efficaces qui permettent d'obtenir des informations sur le fonctionnement même des cellules.
- Le recours à
des plateformes d'imagerie multimodales, c'est-à-dire permettant d'utiliser, consécutivement ou non, plusieurs technologies d'imagerie pour obtenir des données complémentaires sur le plan anatomique, fonctionnel et moléculaire des dysfonctionnements ou pour mettre en oeuvre un traitement de précision en le contrôlant continûment.
-
De nouveaux logiciels et algorithmes de calcul pour le traitement et l'interprétation des images et de l'information sont fondamentaux et indispensables. Ce domaine fait partie intégrante de l'imagerie médicale.
Concernant les applications de l'imagerie médicale, c'est probablement pour l'observation du
cerveau que l'imagerie continuera de jouer un rôle fondamental. Le cerveau est en effet l'un des organes à la fois le plus complexe et le moins accessible du corps humain et l'imagerie médicale permet son observation
in vivo et sans traumatisme.
[1] Un traceur radioactif est une molécule d'intérêt biologique qui est marquée par un radio-isotope qui lui sert d’étiquette. L'instabilité de ce radio-isotope provoque la désintégration qui se traduit par l’émission de rayonnements. Il suffit alors de disposer d’outils de détection appropriés pour suivre à la trace ces radio-isotopes. Le marquage peut être effectué de deux manières : remplacement d’un atome de la molécule par un de ses isotopes radioactifs ou accrochage à la molécule d’un atome radioactif. La molécule marquée est alors un traceur.
[2] Le collimateur est un dispositif placé devant la gamma caméra qui permet de recueillir uniquement les faisceau de photos parallèles entre eux. Il se présente sous la forme d'une plaque en plomb ou tungstène percée de trous cylindriques parfaitement parallèles entre eux.
[3] Il se crée, au moment du passage du message nerveux, une différence ionique, et donc de charges, au niveau de la synapse, zone de connexion entre deux neurones. C'est cette différence de charges, ou différence de potentiels, qui va créer un légère tension électrique locale. C'est l'ensemble de ces micro tensions qui va être mesurable par les électrodes présentes sur le cuir chevelu du patient.