La radioactivité, propriété de certains noyaux d'atomes
Toute matière est constituée d’atomes. Ceux-ci sont composés d’un noyau, contenant des protons et des neutrons, autour duquel orbitent des électrons dont le nombre tend à être égal au nombre de protons. Un type d’atome, appelé élément chimique, est défini et classé selon le nombre de protons dans son noyau. Nous connaissons aujourd’hui 118 éléments, dont 94 naturels. Un type de noyau, appelé nucléide, est défini par son nombre de protons et de neutrons. Un nucléide est stable lorsqu'il comporte un nombre harmonieux de protons et de neutrons ; cette harmonie ne s'observe que pour à peine 10 % des nucléides connus. Les chercheurs ont identifié 256 nucléides stables et près de 3 000 instables. Cette instabilité est due soit à un excès de protons, soit de neutrons, ou encore des deux à la fois.
Les noyaux instables sont dits radioactifs car ils émettent différents types de rayonnements en se transformant. Un type de noyau radioactif est appelé
radionucléide. Pour tendre vers un état stable, les radionucléides se transforment spontanément en d’autres nucléides, radioactifs ou non. Ainsi, de radionucléide en radionucléide,
l’uranium 238 tend à se transformer en un nucléide stable, le plomb 206. La transformation irréversible d’un noyau radioactif en un autre noyau est appelée
désintégration.

Les nucléides se distribuent selon leur nombre de protons et de neutrons ainsi que leur énergie de cohésion sous forme d'une "vallée de stabilité" car le fond est peuplé par les noyaux stables pour lesquels protons et neutrons sont les plus liés. L’évolution des noyaux instables, des hauteurs de la vallée vers le fond, illustre les différents types de radioactivité. © F. Durillon/Animéa
La radioactivité ne concerne que le noyau des atomes alors que les propriétés chimiques des atomes ne dépendent que de leurs électrons (voir le dossier multimédia sur
L'atome).
Les rayonnements émis par les radionucléides sont dits ionisants car ils peuvent arracher des électrons aux atomes de la
matière qu'ils rencontrent et donc en perturber les propriétés chimiques. Un élément chimique correspond à plusieurs nucléides appelés
isotopes qui peuvent être stables ou radioactifs (radio-isotopes). Un isotope porte le nom de son élément chimique, associé à son nombre de neutrons, par exemple le carbone 12 (six neutrons) et le carbone 14 (huit neutrons) sont deux isotopes du carbone (six protons). Le premier n'est pas radioactif, alors que le second l'est. Tous les isotopes ont les mêmes propriétés chimiques alors que leurs propriétés physiques diffèrent un peu, du fait notamment de leur différence de masses.
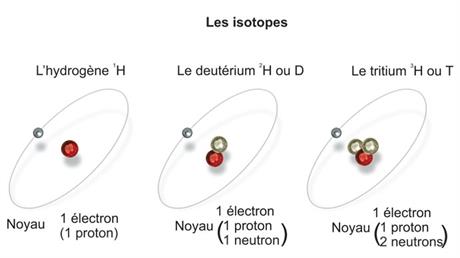
Les isotopes de l'hydrogène. © Yuvanoe
Zoom sur...
La décroissance de l'activité d'un échantillon radioactif en fonction du temps
Au
fur et à mesure que les noyaux se désintègrent, l'activité de
l'échantillon d'un même radionucléide diminue. Les lois du hasard, qui
gouvernent le phénomène de la radioactivité, font qu'au bout d'un temps T
appelé période radioactive, l'activité de l'échantillon a été divisée
par deux. Au bout de deux périodes, il reste un quart des noyaux
radioactifs initiaux. Au bout de trois périodes, un huitième ; au bout
de dix périodes, un millième…

Décroissance de l'activité d'un échantillon radioactif au cours du temps. © Yuvanoé/CEA
la décroissance radioactive
La quantité d'un radionucléide diminue avec le temps du fait de la désintégration radioactive progressive de ses noyaux, phénomène aléatoire et spontané. On peut cependant attribuer à chaque radionucléide une période radioactive, ou demi-vie, qui est le temps au bout duquel la moitié des atomes radioactifs initialement présents s'est désintégrée. La période radioactive est très variable selon le radionucléide : quelques millisecondes, quelques heures, plusieurs jours, des centaines d'années… à des milliards d'années.
La mesure de la radioactivité
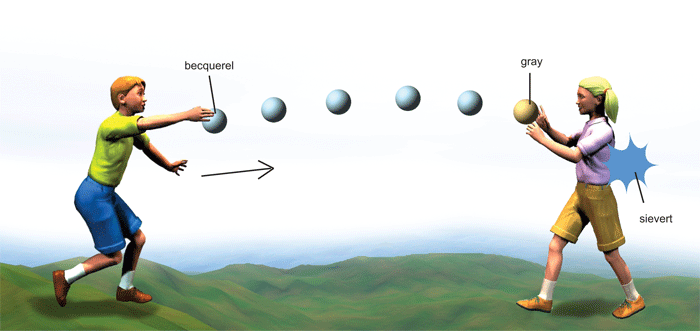
Un enfant lance des ballons en direction d’une camarade. Cette image permet de symboliser la relation entre les trois unités utilisées dans le domaine de la radioactivité. Le nombre de ballons lancés par seconde peut se comparer aux rayonnements résultant des becquerels (nombre de désintégrations par seconde) ; l’énergie reçue par la camarade qui capte les ballons au gray (dose absorbée) ; les effets de cette énergie sur son corps, selon la masse des ballons et l’énergie avec laquelle chacun est envoyé, au sievert (effet produit par la dose absorbée). © Yuvanoe
Différents types de détecteurs mesurent les rayonnements émis par les radionucléides ; parmi eux, des tubes remplis de gaz (chambre d'ionisation, compteur proportionnel, compteur Geiger-Müller), des scintillateurs couplés à des photomultiplicateurs, des diodes de semi-conducteurs (silicium, germanium…).
Ces détecteurs sont extrêmement sensibles et mesurent couramment des activités un million de fois inférieures aux niveaux qui pourraient avoir des effets sur notre santé.
Plusieurs unités sont utilisées dans le domaine de la radioactivité.
Le becquerel (Bq)
Un échantillon radioactif se caractérise par son activité qui est le nombre
de désintégrations de noyaux radioactifs qui se produisent en son sein par seconde. L’unité d’activité est le becquerel, de symbole Bq.
Cette unité est très petite : 1 Bq = 1 désintégration par seconde.
L’activité des sources radioactives s’exprime donc le plus souvent en multiples du becquerel :
- le kilobecquerel (kBq) = 1 000 Bq
- le mégabecquerel (MBq) = 1 million de Bq
- le gigabecquerel (GBq) = 1 milliard de Bq
- le térabecquerel (TBq) = 1 000 milliards de Bq
Le gray (Gy)
Cette unité chiffre la densité d'énergie déposée par les rayonnements dans un organisme ou un objet exposé à un échantillon radioactif. On parle de dose absorbée.
1 gray = 1 joule par kilogramme de matière irradiée.
Le sievert (Sv)
Les effets biologiques, résultant de la dose absorbée par un organisme vivant, varient selon la nature et l'énergie des rayonnements ainsi que sa radiosensibilité. Ces effets se mesurent en sievert, unité qui traduit un équivalent de dose. Cette unité étant très grande, on utilise plutôt :
- le millisievert (mSv) = 1 millième de sievert
- le microsievert (μSv) = 1 millionième de sievert
Le curie (Ci)
C’est l’ancienne unité d’activité qui correspondait à celle d’un gramme de radium 226, radionucléide naturel présent dans les sols. Cette unité est beaucoup plus grande que le becquerel.
1 curie = 37 milliards de becquerels.
Période de quelques isotopes radioctifs d'éléments chimiques

Les principaux types de désintégrations
Radioactivité alpha
Les radionucléides trop chargés à la fois en protons et en neutrons émettent souvent un rayonnement alpha, un noyau d’hélium 4 (2 protons et 2 neutrons, portant 2 charges positives) avec une très grande énergie. Le nucléide initial se transmute en isotope d’un autre élément chimique plus léger. Par exemple, l’uranium 238 est radioactif alpha et se transforme en thorium 234.
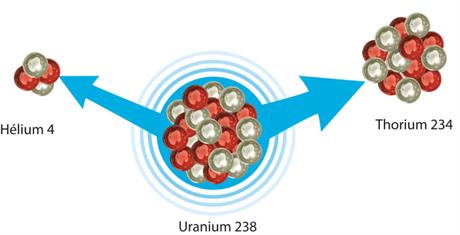
Radioactivité alpha © Yuvanoé/CEA
Radioactivité bêta moins
Le rayonnement bêta moins est constitué d’un électron, chargé négativement. Certains atomes, dont les noyaux sont trop chargés en neutrons, émettent un rayonnement bêta moins : un des neutrons se transforme spontanément en un proton plus un électron, ce dernier étant éjecté avec une grande énergie. Là encore, le nucléide initial s’est transformé en un autre nucléide, isotope d’un autre élément chimique. Par exemple, le strontium 90 est radioactif bêta moins et se transforme en yttrium 90.

Radioactivité bêta - © CEA/Yuvanoé
Radioactivité bêta plus
Le rayonnement bêta plus est constitué d’un
positron (ou positon). Certains atomes, dont les noyaux sont trop chargés en protons, émettent un rayonnement bêta plus : un des protons se transforme spontanément en un neutron plus un positon, ce dernier étant éjecté avec une grande énergie. Ainsi l’atome s’est transformé en un autre élément chimique. Par exemple, l’oxygène 15 est un radioactif bêta plus et se transforme en azote 15.
La radioactivité gamma
Le rayonnement gamma est une onde électromagnétique comme la lumière visible ou les rayons X, mais beaucoup plus énergétique. Ce rayonnement suit souvent une désintégration bêta voire alpha. Après l’émission de la particule alpha ou bêta, le noyau résiduel est encore excité car ses protons et ses neutrons n’ont pas trouvé leur équilibre. Il se libère alors rapidement du trop-plein d’énergie par émission d’un ou plusieurs rayonnements gamma. Par exemple, le cobalt 60 se transforme par désintégration bêta moins en nickel 60 dans un état excité, qui se désexcite ensuite par émission en cascade de deux rayonnements gamma d'énergies d'environ un million de fois plus grandes que celle des photons de lumière visible.
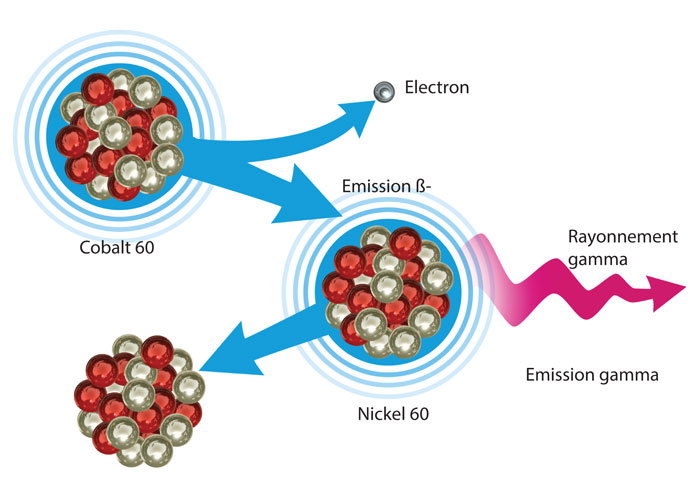
Le rayonnement gamma © Yuvanoé/CEA